
Back Kovalente binding Afrikaans Enlace covalent AN رابطة تساهمية Arabic Enllaz covalente AST Kovalent əlaqə Azerbaijani Кавалентная сувязь Byelorussian Ковалентна връзка Bulgarian সমযোজী বন্ধন Bengali/Bangla Enllaç covalent Catalan Gê̤ṳng-gá-giông CDO
Ovaj članak ili neki od njegovih odlomaka nije dovoljno potkrijepljen izvorima (literatura, veb-sajtovi ili drugi izvori). |
Kovalentna veza je vrsta veze između dva ili više atoma nemetala kojom se između njih postiže neutralna elektronska konfiguracija (konfiguracija plemenitih plinova). Neutralna "kolekcija" atoma vezanih kovalentnom vezom nazvana je molekula. Razlika kovalentne i ionske veze ogleda se u tome što atomi u ionskoj vezi otpuštaju ili primaju elektrone da bi upotpunili svoju elektronsku konfiguraciju do konfiguracije najbližeg plemenitog plina. Nasuprot njih, atomi u kovalentnoj vezi ne otpuštaju elektrone nego ih dijele između sebe i na taj način dostižu elektronsku konfiguraciju najbližeg plemenitog plina.
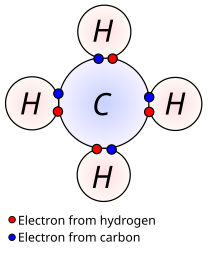
Najjednostavniji način za predstavljanje kovalentne veze u molekuli je tzv. "Lewisova" struktura ili struktura elektronskih tačaka, u kojoj su valentni elektroni atoma predstavljeni kao tačke. Tako naprimjer, vodonik svoj 1s elektron predstavlja jednom tačkom, ugljik ima četiri tačke (2s2 2p2), kisik ima šest tačaka (2s2 2p4) itd. Stabilna molekula se postiže samo onda kada svi atomi u molekuli postignu konfiguraciju plemenitog plina: oktet (osam elektrona) za većinu atoma, odnosno dva za vodik.
U molekuli, nije neophodno da svi elektroni na najvišem energetskom nivou (elektronskoj ljusci) budu uključeni u formiranje kovalentne veze. Valentni elektroni koji ne učestvuju u kovalentnoj vezi nazivaju se usamljeni elektronski parovi (engleski: lone-pair electrons). Na primjer, atom dušika u molekuli amonijaka dijeli šest valentnih elektrona u tri kovalentne veze (sa tri atoma vodika), a preostala dva valentna elektrona su nevezani usamljeni elektroni.
Pored Lewisovog načina predstavljanja kovalentne veze putem tačaka, postoji još i Kekulé-ov model ili linearna struktura prikaza veze. Ovim načinom se umjesto dva kovalentna elektrona između atoma prikazuje prava linija, dok se usamljeni elektronski parovi često izostavljaju.