
Back ان-فورمیلمتیونین AZB N-formilmetionin BS N-Formilmetionina Catalan N-formylmethionin Czech N-Formylmethionine English N-Formilmetionina Spanish ان-فورمیلمتیونین Persian N-Formylméthionine French N-formilmetionina Galician FMET Italian
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||
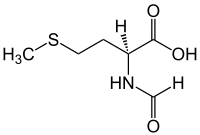
| Strukturformel von N-Formyl-L-methionin | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | N-Formylmethionin | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C6H11NO3S | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 177,22 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
N-Formylmethionin (fMet,[4] HCO-Met,[5] For-Met[5]) ist ein Derivat der Aminosäure Methionin, das an seiner Amino-Gruppe eine zusätzliche Formyl-Gruppe trägt. Bei dem fMet, das in der Proteinsynthese zur Bildung von Proteinen eingesetzt wird, handelt es sich um das Stereoisomer N-Formyl-L-methionin.
fMet wird zur Initiation der Proteinsynthese (Translation) bei den Bacteria, Mitochondrien und Chloroplasten verwendet und kann posttranslational entfernt werden. Es ist deshalb bei diesen Mikroorganismen und Organellen eine proteinogene Aminosäure. Zur Initiation der zytosolischen Proteinsynthese in den Eukaryoten, bei der aus dem eukaryotischen Zellkern stammende Gene translatiert werden, wird anstatt von fMet das Methionin verwendet. Auch Archaea verwenden anstatt von fMet das Methionin zur Initiation der Proteinsynthese.
Im menschlichen Körper wird fMet vom Immunsystem entweder als fremdes Material erkannt oder als ein Alarmsignal, das aufgrund des Austritts von fMet aus beschädigten körpereigenen Zellen ausgelöst wird und den Körper veranlasst, gegen eine potentielle Infektion vorzugehen.
- ↑ a b c Datenblatt N-Formyl-L-methionin bei Sigma-Aldrich, abgerufen am 15. Juni 2022 (PDF).
- ↑ CAS Common Chemistry. Abgerufen am 17. Juni 2022.
- ↑ CAS Common Chemistry. Abgerufen am 27. Mai 2022.
- ↑ Jeremy M. Berg, John L. Tymoczko, Lubert Stryer: Stryer Biochemie. Springer Berlin Heidelberg, Berlin, Heidelberg 2013, ISBN 978-3-8274-2988-9, doi:10.1007/978-3-8274-2989-6.
- ↑ a b Nomenclature and Symbolism for Amino Acids and Peptides, 3AA-18 and 3AA-19