
Back Nitroësuur Afrikaans حمض النتروز Arabic Nitrit turşusu Azerbaijani نیترو اسید AZB Азоцістая кіслата Byelorussian Азотиста киселина Bulgarian নাইট্রাস অ্যাসিড Bengali/Bangla Àcid nitrós Catalan Kyselina dusitá Czech Азотла йӳçек CV
| Acide nitreux | |
 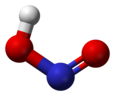  Structure de l'acide nitreux cis et trans. |
|
| Identification | |
|---|---|
| Nom UICPA | acide nitreux nitrite d'hydrogène |
| No CAS | |
| No ECHA | 100.029.057 |
| No CE | 231-963-7 |
| PubChem | 24529 |
| ChEBI | 25567 |
| SMILES | |
| InChI | |
| Apparence | solution bleu pâle |
| Propriétés chimiques | |
| Formule | HNO2 [Isomères] |
| Masse molaire[2] | 47,013 4 ± 0,000 9 g/mol H 2,14 %, N 29,79 %, O 68,06 %, |
| pKa | 3.35 à 25 °C |
| Moment dipolaire | 1,423 ± 0,005 D (cis) 1,855 ± 0,016 D (trans)[1] |
| Propriétés électroniques | |
| 1re énergie d'ionisation | ≤ 11,3 eV (gaz)[3] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
L'acide nitreux (HONO) est un composé chimique de formule HNO2. C'est un monoacide faible que l'on ne connaît qu'en solution pas trop acide (il se dismute au pH bas), et en phase gazeuse. Ses sels (les nitrites) sont stables en solution aqueuse. L'acide nitreux est un des réactifs essentiels de la préparation des colorants azoïques et, dans l'air, le précurseur du radical hydroxyle (OH), l'un des principaux polluant de l'air, et une espèce chimique clé dans la formation des épisodes de pollution photochimique (c'est un puissant photo-oxydant).
En laboratoire, il et préparé in situ par acidification de nitrite de sodium à basse température (environ 5 °C).
La molécule HNO2 a été détectée dans le milieu interstellaire dans la composante B du système binaire IRAS 16293−2422 (en)[4].
- (en) David R. Lide, Handbook of chemistry and physics, CRC, , 89e éd., 2736 p. (ISBN 142006679X et 978-1420066791), p. 9-50
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) David R. Lide, Handbook of chemistry and physics, CRC, , 89e éd., 2736 p. (ISBN 978-1-4200-6679-1), p. 10-205
- (en) A. Coutens, N. F. W. Ligterink, J.-C. Loison, V. Wakelam, H. Calcutt, M. N. Drozdovskaya, J. K. Jørgensen, H. S. P. Müller, E. F. van Dishoeck et S. F. Wampfler, « The ALMA-PILS survey: First detection of nitrous acid (HONO) in the interstellar medium », Astronomy & Astrophysics, vol. 623, , article no L13 (DOI 10.1051/0004-6361/201935040, Bibcode 2019A&A...623L..13C, arXiv 1903.03378, lire en ligne)