
Back عدد كمي Arabic Númberu cuánticu AST Квантавы лік Byelorussian Квантово число Bulgarian কোয়ান্টাম সংখ্যা Bengali/Bangla Kvantni broj BS Nombre quàntic Catalan Kvantové číslo Czech Квантла хисеп CV Quantenzahl German
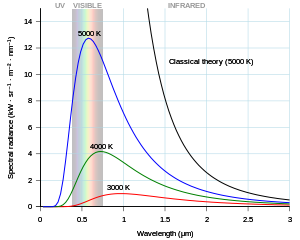







Kvantni broj je broj koji opisuje kvantnomehaničko stacionarno stanje subatomskih čestica, elektrona u atomu i nukleona (protona i neutrona) u atomskoj jezgri. Kvant i kvantni broj u fiziku je uveo M. Planck 1900. kako bi objasnio raspodjelu energije zračenja crnoga tijela i uskladio zakone klasične fizike s pokusima. U modernoj fizici pod pojmom kvantizacije podrazumijeva se prijelaz iz zakonitosti klasične fizike u kvantnu mehaniku. Kvantiziranje gravitacije jedan je od najvećih problema suvremene fizike elementarnih čestica i kozmologije.
Tipično je značenje kvantnih brojeva stanjâ elektrona u atomu sljedeće:
- glavni kvantni broj n određuje svojstvene vrijednosti energije elektrona,
- orbitalni kvantni broj l određuje vrijednost kutne količine gibanja elektrona u kvantnim stazama,
- magnetski kvantni broj m određuje moguće orijentacije kutne količine gibanja u odnosu na os vanjskoga magnetskoga polja,
- kvantni broj spina s određuje spinsku kutnu količinu gibanja elektrona.
Ukupni broj različitih stanja u atomu za kvantne brojeve n, l i m iznosi (2∙l + 1), a zbog dviju spinskih orijentacija (projekcija) na vanjsku os taj se broj udvostručuje. Stanja elektrona u modelu Fermijeva plina opisana su samo glavnim kvantnim brojem n i s dvije orijentacije spina. Kvanti svjetlosti (fotoni), kao bozoni cjelobrojnoga spina opisani su Bose-Einsteinovom statistikom, a istoj statistici podvrgavaju se i kvanti titranja kristalne rešetke (fonon) kao bozoni nultoga spina. Neutroni i protoni, šire hadroni, uz kvantni broj spina imaju još i kvantni broj izospina. Uz spin i okus (gornji, donji, strani …), kvarkovi nose i kvantni broj jakoga naboja, koji se uobičajeno naziva bojom (crvena, zelena, plava), a antikvarkovi odgovarajuću antiboju. Teorija polja boje u kvantnome obliku poznata je kao kvantna kromodinamika.[1]