
Back Karbonaat Afrikaans كربونات Arabic Carbonatu AST Karbonatlar Azerbaijani کربونات AZB Карбонат Bulgarian Karbonat BS Carbonat Catalan Uhličitany Czech Карбонат CV
| |
| Nama | |
|---|---|
| Nama IUPAC (sistematis)
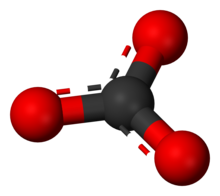
Karbonat | |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| UNII | |
| |
| |
| Sifat | |
| CO2−3 | |
| Massa molar | 60,01 g·mol−1 |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Karbonat merupakan suatu garam dari asam karbonat (H2CO3),[1] yang dicirikan oleh adanya ion karbonat, suatu ion poliatomik dengan rumus CO2−3. Nama ini juga berarti suatu ester dari asam karbonat,[1] suatu senyawa organik yang mengandung gugus karbonat C(=O)(O–)2.
Istilah ini juga digunakan sebagai kata kerja, untuk menggambarkan karbonasi: proses meningkatkan konsentrasi ion karbonat dan bikarbonat dalam air untuk menghasilkan air berkarbonasi dan minuman berkarbonasi lainnya. – baik dengan penambahan gas karbon dioksida di bawah tekanan, atau dengan melarutkan karbonat atau garam bikarbonat ke dalam air.
Dalam geologi dan mineralogi, istilah "karbonat" dapat merujuk ke mineral karbonat dan batu karbonat[2] (yang terbuat dari mineral karbonat), dan keduanya didominasi oleh ion karbonat, CO2−3. Mineral karbonat sangat bervariasi dan di mana-mana diendapkan secara kimia batuan sedimen. Yang paling umum adalah kalsit[3] atau kalsium karbonat, CaCO3, penyusun utama batu kapur (dan juga komponen utama kerang moluska dan kerangka terumbu karang; dolomit,[4] kalsium magnesium karbonat CaMg(CO3)2; dan siderit,[5] atau besi(II) karbonat, FeCO3, suatu bijih besi yang penting. Natrium karbonat ("soda" atau "natron") dan kalium karbonat ("kalium") telah digunakan sejak zaman purba untuk pembersihan dan pelestarian, dan juga untuk pembuatan kaca. Karbonat banyak digunakan dalam industri, misalnya dalam peleburan besi, sebagai bahan baku pembuatan semen Portland dan pembuatan kapur, dalam komposisi glasir keramik, dan banyak lagi.
- ^ a b
 Chisholm, Hugh, ed. (1911). "Carbonates". Encyclopædia Britannica (edisi ke-11). Cambridge University Press.
Chisholm, Hugh, ed. (1911). "Carbonates". Encyclopædia Britannica (edisi ke-11). Cambridge University Press.
- ^ Murray, C. L. (1960). "Origin of porosity in carbonate rocks". Journal of Sedimentary Research. 30 (1): 59–84. doi:10.1306/74D709CA-2B21-11D7-8648000102C1865D.
- ^ Serway, R.A.; Marshall, S.A. (1967). "Electron Spin Resonance Absorption Spectra of C03 and CO3-3 Molecular Ions in Irradiated Single-crystal Calcite". J. Chem. Phys. 46: 1949–1952. doi:10.1063/1.1840958.
- ^ Gisquet, F.; Lamarche, J.; Floquet, M.; Borgomano, J.; Masse, J.; Caline, B. (2013). "Three-dimensional structural model of composite dolomite bodies in folded area (Upper Jurassic of the Etoile massif, southeastern France)". AAPG Bulletin. 97: 1477–1501. doi:10.1306/04021312016.
- ^ Ha, J.; Zhao, X.; Yu, R.; Barkay, T.; Yee, N. (2017). "Hg(II) reduction by siderite (FeCO3)". Applied Geochemistry. 78: 211–218. doi:10.1016/j.apgeochem.2016.12.017.