Back ثنائي الفوسفان Arabic Difosfan Azerbaijani دیفوسفان AZB Difosfà Catalan Difosfan Czech Diphosphan German Διφωσφίνη Greek Diphosphane English Difosfano Spanish دیفسفان Persian
| |||||||||||||||
| |||||||||||||||
| Ogólne informacje | |||||||||||||||
| Wzór sumaryczny |
P | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Inne wzory |
H | ||||||||||||||
| Masa molowa |
65,98 g/mol | ||||||||||||||
| Wygląd |
bezbarwna ciecz[2] | ||||||||||||||
| Identyfikacja | |||||||||||||||
| Numer CAS | |||||||||||||||
| PubChem | |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| Podobne związki | |||||||||||||||
| Podobne związki | |||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||
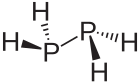
Difosfina, P
2H
4 – nietrwały nieorganiczny związek chemiczny, połączenie fosforu i wodoru o budowie chemicznej analogicznej do hydrazyny (H
2N−NH
2). Jest bezbarwną cieczą ulegającą spontanicznemu zapłonowi w powietrzu. Zawartość difosfiny w fosfinie jest przyczyną jej samozapłonu w powietrzu o temperaturze pokojowej. Difosfina posiada charakterystyczny zapach zgniłych ryb – wyczuwalny nawet przy bardzo niskich stężeniach.
Difosfinę otrzymać można przez hydrolizę fosforku wapnia (Ca
3P
2) w obniżonej temperaturze i oddzielenie od fosforiaku[3][4]. Powstaje jako produkt uboczny w procesie otrzymywania fosfiny[5]. Może powstawać także podczas rozkładu materii organicznej i według niektórych hipotez, difosfina powstająca w ten sposób przyczynia się do występowania błędnych ogników[6].
- ↑ Błąd w przypisach: Błąd w składni elementu
<ref>. Brak tekstu w przypisie o nazwieRedBookBŁĄD PRZYPISÓW - ↑ a b c d e Błąd w przypisach: Błąd w składni elementu
<ref>. Brak tekstu w przypisie o nazwieCRCBŁĄD PRZYPISÓW - ↑ Błąd w przypisach: Błąd w składni elementu
<ref>. Brak tekstu w przypisie o nazwieTołłoczkoBŁĄD PRZYPISÓW - ↑ Błąd w przypisach: Błąd w składni elementu
<ref>. Brak tekstu w przypisie o nazwieBaudlerBŁĄD PRZYPISÓW - ↑ Błąd w przypisach: Błąd w składni elementu
<ref>. Brak tekstu w przypisie o nazwieBielański2010BŁĄD PRZYPISÓW - ↑ Błąd w przypisach: Błąd w składni elementu
<ref>. Brak tekstu w przypisie o nazwieŻychowskiBŁĄD PRZYPISÓW