
Back Redoksreaksie Afrikaans أكسدة واختزال Arabic Amenorgamientu-oxidación AST Окисланыу-ҡайтарылыу реакциялары Bashkir Акісляльна-аднаўленчыя рэакцыі Byelorussian Затляняльна-аднаўленчыя рэакцыі BE-X-OLD Окислително-редукционни процеси Bulgarian জারণ Bengali/Bangla Redoks-reakcija BS Reacció d'oxidació reducció Catalan
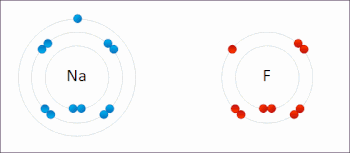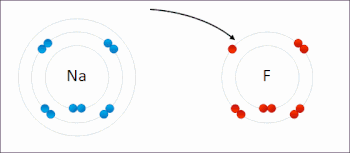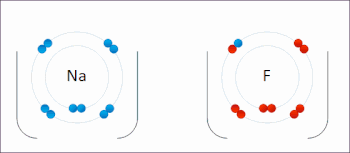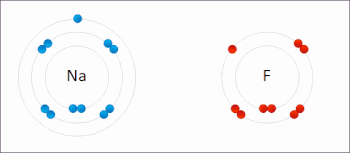
Redoks atomların oksidasyon durumlarının değiştiği bir tür kimyasal reaksiyondur. Redoks reaksiyonları, kimyasal türler arasında elektronların fiili veya biçimsel aktarımı ile karakterize edilir, çoğunlukla bir tür (indirgeyici ajan) oksidasyona (elektronları kaybeden), diğer türler (oksitleyici ajan) indirgemeye uğrar (elektron kazanır).[1] Elektronun çıkarıldığı kimyasal türlerin indirgenmiş olduğu söyleniyor. Başka bir deyişle:
- Oksidasyon, elektronların bir atom ya da molekülden ayrılmasını sağlayan kimyasal tepkimedir.
- Redüksiyon, bir atomun elektron almasını sağlayan kimyasal tepkimedir.
Organik kimyadaki birçok reaksiyon, oksidasyon durumlarındaki değişikliklerden kaynaklanan, ancak farklı elektron transferi olmaksızın redoks reaksiyonlarıdır. Örneğin ahşabın moleküler oksijen ile yanması sırasında odun içerisindeki karbon atomlarının oksidasyon durumu artmakta ve karbondioksit ve su oluştukça oksijen atomlarının oksidasyon durumu azalmaktadır. Oksijen atomları indirgenir, resmen elektron kazanır, karbon atomları ise oksidasyona uğrayarak elektron kaybeder. Dolayısıyla bu reaksiyonda oksijen oksitleyici madde ve karbon indirgeyici maddedir.[2]
Oksidasyon reaksiyonları genellikle oksijen moleküllerinden oksitlerin oluşumu ile ilişkilendirilse de, diğer kimyasal türler de aynı işlevi görebileceğinden, oksijen bu tür reaksiyonlara dâhil edilmez.[2]
Redoks reaksiyonları, pas oluşumunda olduğu gibi nispeten yavaş veya yanan yakıt durumunda olduğu gibi çok daha hızlı gerçekleşebilir. Karbon dioksit (CO2) elde etmek için karbonun oksidasyonu veya metan (CH4) elde etmek için karbonun hidrojenle indirgenmesi gibi basit redoks prosesleri ve insan vücudunda glikoz oksidasyonu (C6H12O6) gibi daha karmaşık prosesler vardır. Sudaki bağ enerjilerinin ve iyonlaşma enerjilerinin analizi redoks potansiyellerinin hesaplanmasına izin verir.[3][4]
- ^ "Concepts in Biochemistry - Concept Reviews". www.wiley.com. 13 Aralık 2009 tarihinde kaynağından arşivlendi. Erişim tarihi: 7 Ocak 2021.
- ^ a b "Gale In Context: Science - Document - Oxidation-reduction reaction". go.gale.com. 12 Kasım 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 7 Ocak 2021.
- ^ Schmidt-Rohr, Klaus (9 Ekim 2018). "How Batteries Store and Release Energy: Explaining Basic Electrochemistry". Journal of Chemical Education. 95 (10): 1801-1810. doi:10.1021/acs.jchemed.8b00479. ISSN 0021-9584.
- ^ Schmidt-Rohr, Klaus (8 Aralık 2015). "Why Combustions Are Always Exothermic, Yielding About 418 kJ per Mole of O2". Journal of Chemical Education. 92 (12): 2094-2099. doi:10.1021/acs.jchemed.5b00333. ISSN 0021-9584.