
Back Diffusie Afrikaans انتشار Arabic Diffuziya Azerbaijani Дыфузія Byelorussian Дыфузія BE-X-OLD Дифузия Bulgarian ব্যাপন Bengali/Bangla Difuzija BS Difusió Catalan بڵاوبوونەوە CKB

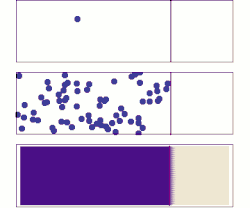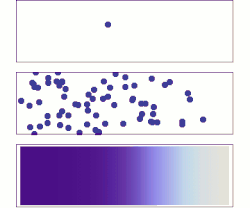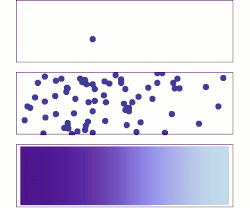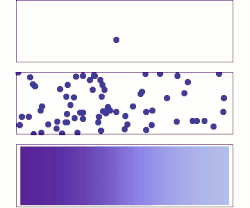

Dyfuzja (łac. diffusio „rozprzestrzenianie”) – proces samorzutnego rozprzestrzeniania i przenikania się cząsteczek lub energii w każdym ośrodku (o temperaturze > 0 K) (np. w gazie, cieczy lub ciele stałym itd.), będący konsekwencją chaotycznych zderzeń cząsteczek dyfundującej substancji między sobą lub z cząsteczkami otaczającego ją ośrodka[1].
Ze względu na skalę zjawiska, rozpatruje się dwa podstawowe rodzaje dyfuzji:
- dyfuzja śledzona (ang. tracer diffusion) – proces mikroskopowy polegający na chaotycznym ruchu pojedynczej („śledzonej”) cząsteczki (przykład: ruchy Browna),
- dyfuzja chemiczna – proces makroskopowy obejmujący makroskopowe ilości materii (lub energii), zwykle opisywany równaniem dyfuzji i prowadzący do wyrównywania stężenia (lub temperatury) każdej z dyfundujących substancji w całym układzie.
Podstawowymi prawami opisującymi dyfuzję są prawa Ficka. Pierwsze prawo Ficka stwierdza że:
- strumień cząstek dyfuzji jest proporcjonalny do ujemnego gradientu stężenia
gdzie:
- – gęstość strumienia składnika (masa molowa składnika przepływająca przez jednostkowy przekrój w jednostce czasu),
- – współczynnik dyfuzji,
- – stężenie [(ilość substancji) na jednostkę objętości],
- – współrzędna osi, wzdłuż której zachodzi dyfuzja.
W ogólnym, trójwymiarowym przypadku wzór można zapisać niezależnie od współrzędnych:
Dla chemicznej dyfuzji materii (masy) współczynnik dyfuzji jest nazywany współczynnikiem dyfuzji molekularnej. Dla tej samej substancji, w tych samych warunkach, współczynniki dyfuzji śledzonej i chemicznej są zwykle różne, gdyż drugi z tych współczynników uwzględnia oddziaływania i korelacje pomiędzy trajektoriami poszczególnych dyfundujących cząsteczek.
Dyfuzja zachodzi zarówno w stanie równowagi, jak i poza równowagą termodynamiczną. Dyfuzję śledzoną bada się zwykle w stanie równowagi, a dyfuzję chemiczną w układach nierównowagowych. Dyfuzja w stanie braku równowagi termodynamicznej jest procesem nieodwracalnym, który przybliża stan układu do stanu równowagi termodynamicznej i zwiększa jego entropię. Dyfuzja chemiczna zachodząca w stanie równowagi zwana jest samodyfuzją.
Dyfuzja materii jest zjawiskiem aktywowanym termicznie – zwiększenie temperatury zwykle prowadzi do zwiększenia tempa dyfuzji. W przypadku większości ciał stałych zależność tę opisuje równanie Arrheniusa.
Dyfuzja jest jednym z mechanizmów transportu. W tym kontekście jej bardzo charakterystyczną cechą jest to, że typowa odległość o którą przemieszczana jest substancja z obszaru o podwyższonym stężeniu po dostatecznie długim czasie jest proporcjonalna do pierwiastka kwadratowego z czasu:
Dla większości substancji powyższa zależność obowiązuje (dla dostatecznie dużych czasów ) nawet wtedy, gdy współczynnik dyfuzji danej substancji zależy od jej stężenia. W pewnych układach obserwuje się jednak procesy, które w obrazie mikroskopowym składają się z szeregu charakterystycznych dla dyfuzji „chaotycznych” zderzeń, w których to jednak procesach obowiązuje zależność
W takich przypadkach mówi się o dyfuzji anomalnej.
Dyfuzja może też dotyczyć energii, jej szybkość jest określona przez współczynnik dyfuzji termicznej. Na przykład źródłem niekonwekcyjnego i nieradiacyjnego transportu ciepła jest wymiana energii kinetycznej pomiędzy chaotycznie zderzającymi się cząsteczkami, stąd też równanie przewodnictwa cieplnego w ciałach stałych jest tożsame równaniu dyfuzji.
W przypadku dyfuzji pędu, o szybkości procesu dyfuzji decyduje współczynnik dyfuzji zwany lepkością kinematyczną, czyli współczynnikiem tarcia wewnętrznego.
- ↑ Dyfuzja, [w:] Encyklopedia PWN [online], Wydawnictwo Naukowe PWN [dostęp 2021-07-22].










